ÁCIDOS CARBOXILICO
¿Qué
son?
Se
caracterizan por tener el grupo
"carboxilo" -COOH en el extremo de la
cadena.
PROPIEDADES FÍSICAS Y
USOS DE LOS ÁCIDOS CARBOXILICOS
Los ácidos carboxílicos se emplean en la producción de
polímeros
farmacéuticos
solventes y aditivos
ácido acético (elaboración de vinagre)
BENEFICIOS Y RIESGOS PARA
LA SALUD
Los ácidos carboxílicos nos
benefician en la estética como se puede encontrar en los labiales, en la formación
de polímeros los cuales nos ayudan a tener una vida más practica con sus plásticos
para guardar alimentos y tan bien justo con eso se ve en los aditivos y
solventes de los productos alimenticios, los ácidos carboxílicos se encuentran
tan bien en los productos de laboratorio como lo son las medicinas, se puede
encontrar muy común mente en los vinagres tan bien se puede encontrar en las
hormigas las cuales forman el ácido fórmico con el cual si se tiene contacto
puede dar irritación en cualquier parte que este tenga contacto con el cuerpo.
NOMENCLATURA
Se
nombran anteponiendo la palabra "ácido" al nombre del
hidrocarburo del que proceden y con la terminación
"-oico".
ácido etanoico
Son numerosos los ácidos
dicarboxílicos, que se nombran con la terminación "-dioico"
ácido
propanodioico
Con frecuencia se sigue utilizando el
nombre tradicional, aceptado por la IUPAC, para muchos de ellos, fíjate en los
ejemplos.
Cuando los grupos carboxílicos se
encuentran en las cadenas laterales, se nombran utilizando el prefijo
"carboxi-" y con un número localizador de esa función. Aunque en el
caso de que haya muchos grupos ácidos también se puede nombrar el compuesto
posponiendo la palabra "tricarboxílico",
"tetracarboxílico", etc., al hidrocarburo del que proceden.
ácido
2-carboxipentanodioico o ácido 1,1,3-propanotricarboxílico
Ejemplos
ác. metanoico (ác. fórmico)
ác. etanoico (ác. acético)
ác. propenoico
ác.
benceno-carboxílico (ác. benzoico)
ác. propanodioico (ác. malónico)
1,1,3-propanotricarboxílico
BIBLIOGRAFIA
http://www.alonsoformula.com/organica/acidos_carboxilicos.htm
https://www.youtube.com/watch?v=A8y2eUeIJP8
https://www.youtube.com/watch?v=o143jhHVn0g
http://espanol.answers.yahoo.com/question/index?qid=20120519131710AAlRBtv
http://mx.selecciones.com/upload/contents/secondaryImage_1187.jpg
http://blog.purenature.es/wp-content/imagescaler/74a1fc7e27a0756b0c76dc08a27798c6.jpg
http://www.webadicto.net/image.axd?picture=registro-sanitario-de-medicamentos-en-peru_1.jpg
http://www.inti.gob.ar/plasticos/imagenes/campos.jpg



.jpg)











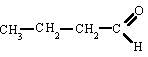 butanal
butanal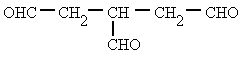 3-formilpentanodial
3-formilpentanodial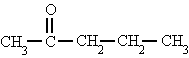 metil propil cetona
metil propil cetona